المناعة الشخصية: نهاية الجرعات العشوائية في علاج رفض الأعضاء
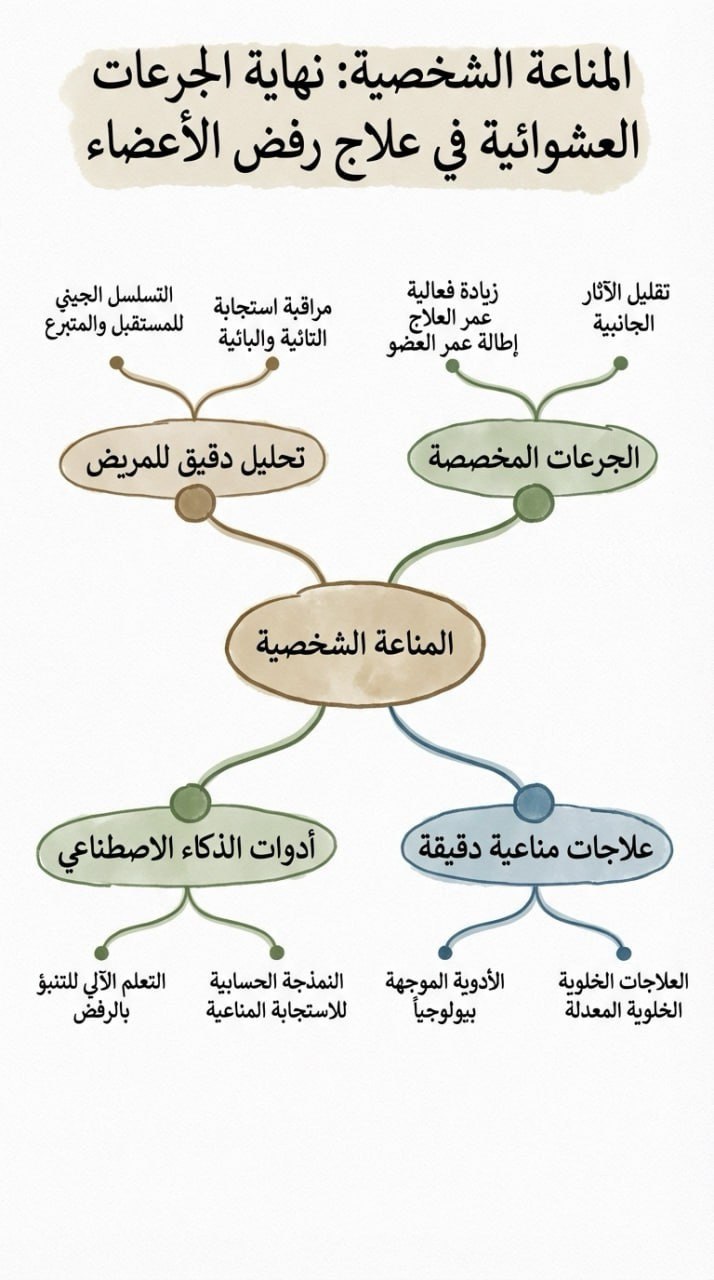
المناعة الشخصية: نهاية الجرعات العشوائية في علاج رفض الأعضاء
مقدمة: التحدي المزدوج لمثبطات المناعة
تعتبر زراعة الأعضاء إحدى أعظم إنجازات الطب الحديث، حيث تمنح المرضى فرصة ثانية للحياة. ومع ذلك، فإن نجاح هذه العملية يعتمد بشكل حاسم على قدرة الأطباء على إدارة التحدي الأكبر: الرفض المناعي. ولتحقيق ذلك، يتناول المرضى مدى الحياة أدوية مثبطة للمناعة قوية.
هذه الأدوية، رغم أهميتها، تضع المرضى أمام تحدٍ مزدوج: فإما أن تكون الجرعة منخفضة جداً، مما يؤدي إلى رفض العضو وتلفه، أو تكون عالية جداً، مما يعرض المريض لآثار جانبية خطيرة تشمل العدوى، والسرطان، وتلف الكلى والكبد.
لقد اعتمدت الممارسة الطبية لعقود على نهج “مقاس واحد يناسب الجميع” في تحديد جرعات هذه الأدوية، مع تعديلات بسيطة بناءً على قياس مستويات الدواء في الدم (Therapeutic Drug Monitoring – TDM). لكن هذا النهج لم يعد كافياً في عصر الطب الشخصي (Precision Medicine).
اليوم، يقود خبراء زراعة الأعضاء ثورة حقيقية نحو المناعة الشخصية (Personalized Immunosuppression)، وهي مقاربة تهدف إلى إنهاء عصر الجرعات العشوائية وتوفير العلاج الأمثل لكل مريض على حدة.
لماذا تفشل الجرعات العشوائية؟
تتباين استجابة المرضى بشكل كبير بسبب عدة عوامل، منها:
- العوامل الجينية: تؤثر جينات مثل
CYP3A5وMDR1على استقلاب دواء التاكروليمس. - الخصائص الفردية: مثل العمر، الوزن، وظائف الكبد والكلى، والأدوية المصاحبة.
- النشاط المناعي: إذ يختلف مستوى “عدوانية” الجهاز المناعي من مريض لآخر.
إن قياس تركيز الدواء في الدم وحده لا يعكس تأثيره الفعلي على الخلايا المناعية، مما يجعل الجرعات الحالية غير دقيقة.
المناعة الشخصية: مقاربة ثلاثية الأبعاد
| المحور | الأدوات الرئيسية | الهدف |
|---|---|---|
| 1. علم الجينات (Pharmacogenomics) | تحليل جينات CYP3A5, MDR1, CYP2C19 | تحديد الجرعة الأولية بناءً على الاستقلاب الجيني |
| 2. المؤشرات الحيوية (Biomarkers) | التعبير الجيني، الخلايا التائية التنظيمية (Tregs) | قياس النشاط المناعي الفعلي |
| 3. الذكاء الاصطناعي (AI/ML) | نماذج التعلم الآلي | التنبؤ بالجرعة المثلى |
المؤشرات الحيوية: قراءة لغة المناعة
- اختبارات التعبير الجيني: تكشف عن نشاط الجينات المرتبطة بالرفض المناعي.
- قياس الخلايا التائية التنظيمية (Tregs): انخفاضها يشير إلى زيادة خطر الرفض.
- قياس نشاط إنزيمات مثل Calcineurin و IMPDH: يعطي مؤشراً أدق لفعالية الدواء.
الذكاء الاصطناعي: التنبؤ بالجرعة المثلى
يعمل الذكاء الاصطناعي عبر ثلاث خطوات:
- جمع بيانات المريض (العمر، الوزن، الجينات، مستويات الدواء…)
- تدريب النموذج على آلاف الحالات السابقة.
- إنتاج توصية دقيقة بالجرعة لكل مريض.
وقد أظهرت الدراسات أن هذه النماذج تقلل خطر الرفض وتحسن دقة جرعات التاكروليمس.
الفوائد الملموسة للمناعة الشخصية
| الفئة | الفائدة | الشرح |
|---|---|---|
| للمريض | تقليل الآثار الجانبية | تجنب الجرعات الزائدة التي تسبب مشاكل خطيرة |
| للعضو المزروع | إطالة عمر العضو | تقليل الرفض الحاد والمزمن |
| للطبيب | اتخاذ قرار دقيق | اعتماد بيانات موضوعية |
| للنظام الصحي | توفير التكاليف | تقليل علاج المضاعفات |
دور المملكة والخبراء في تبني الطب الشخصي
يمثل تبني تقنيات الطب الشخصي خطوة تتماشى مع رؤية المملكة 2030. حيث يمكن للخبراء قيادة جهود إدماج اختبارات التعبير الجيني ونماذج الذكاء الاصطناعي في بروتوكولات زراعة الأعضاء، مما يضع المملكة في موقع ريادي إقليمياً.
خاتمة: نحو مستقبل أكثر أماناً ودقة
لقد انتهى عصر الجرعات العشوائية. اليوم، نحن أمام حقبة جديدة تقوم على الدمج بين علم الجينات والمؤشرات الحيوية والذكاء الاصطناعي. المناعة الشخصية ليست مجرد تحسين للعلاج، بل إعادة تصور كاملة للعلاقة بين المريض والدواء.
المراجع
- Cheung, C. Y., et al. (2022). Personalized immunosuppression after kidney transplantation. PubMed.
- Fu, R., et al. (2019). Biomarkers for individualized dosage adjustments in immunosuppressive drugs. Nature.
- Jaksch, P., et al. (2022). Integrated Immunologic Monitoring in Solid Organ Transplantation. Transplant Journal.
- Barcelona Consensus. (2016). Biomarker-based immunosuppressive drugs management. Drug Monitoring.
- Basuli, D., et al. (2023). AI to Predict Immunosuppressive Drug Dosing. PMC.
- Budde, K., et al. (2023). Toward personalized immunosuppression. Kidney International.
